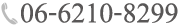当セルバンクで提供している細胞は下記の特徴を有するため、高品質、高安全性が維持され、
他家間葉系幹細胞を用いた迅速で低コストの細胞治療を目指した研究にご使用いただけます※
※非臨床研究グレードの細胞は、ヒトへの使用はできません。
当セルバンクの特徴
■ヒト滑膜由来間葉系幹細胞

- 大阪大学医学部附属病院倫理審査委員会で承認された手順に基づいて、同意取得、同意撤回の機会、ドナースクリーニング、無償提供、提供者の個人情報保護等の様々な条件を遵守して実施
- 大阪大学医学部附属病院未来医療開発部未来医療センターCPCを利用※し、製造・品質管理された体制で細胞調製を行い、全てのデータを厳重に保管しているためトレーサビリティーが容易
※一部、共同研究機関のCPC施設において培養し、手順書に従って阪大に搬入 - 生物由来原料基準(平成15年厚生労働省告示第210号)に則した安全性の高い臨床用無血清培地STK1, 2を使用
- 各工程において工程内管理試験を実施し、全て合格済の細胞を保管
-工程内管理試験の一例
(細胞増殖能、生存率、表面抗原発現、無菌試験、マイコプラズマ否定試験、エンドトキシン試験等) - 感染検査実施済み
感染症検査を実施し、ドナースクリーニングにおいて下記全ての項目に関して陰性であることを確認済み
非臨床研究グレードの細胞
| B型肝炎ウイルス | C型肝炎ウイルス | ヒト細胞白血病ウイルス | サイトメガロウイルス |
| パルボウイルスB19 | エイズウイルス | EBウイルス | マイコプラズマ | 梅毒 |
臨床研究グレードの細胞
| B型肝炎ウイルス | C型肝炎ウイルス | ヒト細胞白血病ウイルス | サイトメガロウイルス | パルボウイルスB19 |
| エイズウイルス | EBウイルス | 風疹ウイルス | ムンプスウイルス | マイコプラズマ | 梅毒 |
- 保管中の細胞は24時間体制で環境モニタリング管理
■ヒトさい帯由来間葉系幹細胞

-
非臨床研究の利用に関するインフォームドコンセントを取得し、無血清培地を使用して製造したヒト臍帯由来間葉系幹細胞の提供を開始しました。
- 製造工程における感染症検査(マイコプラズマ否定試験、エンドトキシン試験、無菌試験)および動物実験に必要な微生物検査に合格済み
- 微生物検査を実施し、下記の項目に関して陰性であることを確認済み
PCR Test (ICLAS Monitoring Center)※
| Clostridium piliforme | Ectromelia virus | LCM virus | Mouse hepatitis virus | Mycoplasma pulmonis | Sendai virus |
| Hepatitis B virus(HBV) | Hepatitis C virus(HCV) | Human T-lymphotropic virus1(HTLV-1) | Human Immunodeficiency virus1(HIV-1) | Treponema pallidum |
※大阪大学医学部附属動物実験施設での生物材料の投与にあたり必要な微生物検査項目を実施しており、そのまま投与できます。
保管中の一部の細胞を用いたデータ
■滑膜由来間葉系幹細胞
増殖能
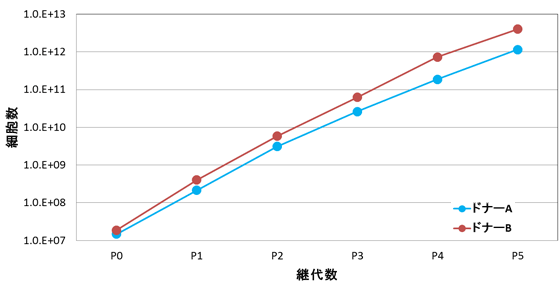
分化能
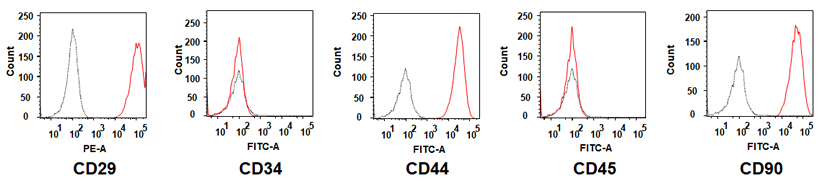
表面抗原マーカー発現
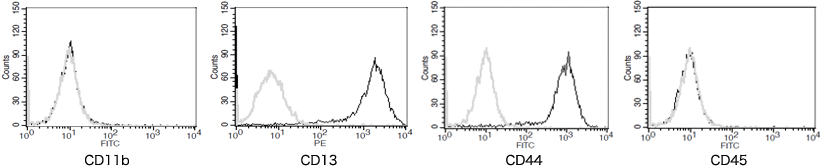
■ヒトさい帯由来間葉系幹細胞
増殖能
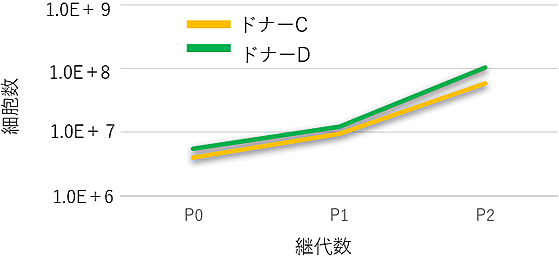
分化能
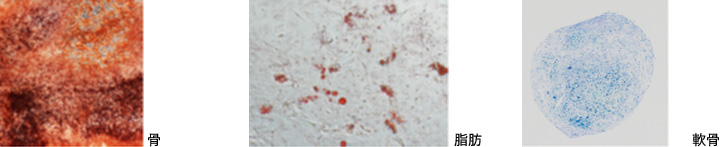
表面抗原マーカー